Das Verdünnen von Lösungen ist in vielen Laboren ein gängiges Verfahren. Kennen Sie das? Man liest Anweisungen wie „100 ml einer verdünnten Lösung herstellen“ und fragt sich: Wo fange ich an? Damit sind Sie nicht allein. Verdünnen gehört zu den häufigsten Verfahren in der Chemie, von Schulpraktika bis hin zur professionellen Forschung. Die gute Nachricht: Sobald man die Logik verstanden hat, wird der Vorgang vorhersehbar und fast schon mechanisch.
Dieser Leitfaden erklärt genau, was Verdünnung bedeutet, wie die Formel funktioniert und wie man eine Verdünnung sicher und korrekt durchführt.
Was bedeutet „eine Lösung verdünnen“?

Verdünnen bedeutet, die Konzentration einer Lösung durch Zugabe von mehr Lösungsmittel, üblicherweise demineralisiertem Wasser , zu verringern. Das Grundprinzip ist einfach:
Man entfernt die gelöste Substanz nicht, sondern verteilt sie über ein größeres Volumen.
Stellen Sie sich vor, Sie geben Wasser in ein Glas Orangensaft. Der Geschmack nimmt ab, aber die Saftmenge bleibt gleich. In der Chemie funktioniert es genau genauso.
Beim Verdünnen einer Lösung:
- Die Menge des gelösten Stoffes bleibt gleich
- Das Gesamtvolumen erhöht sich
- Die Konzentration nimmt ab.
Sobald man dieses Prinzip verstanden hat, werden die Berechnungen wesentlich einfacher.
Die Verdünnungsformel erklärt (C₁V₁ = C₂V₂)
Für die meisten Verdünnungsprobleme verwendet man eine einfache Gleichung:
C₁V₁ = C₂V₂
Das heisst:
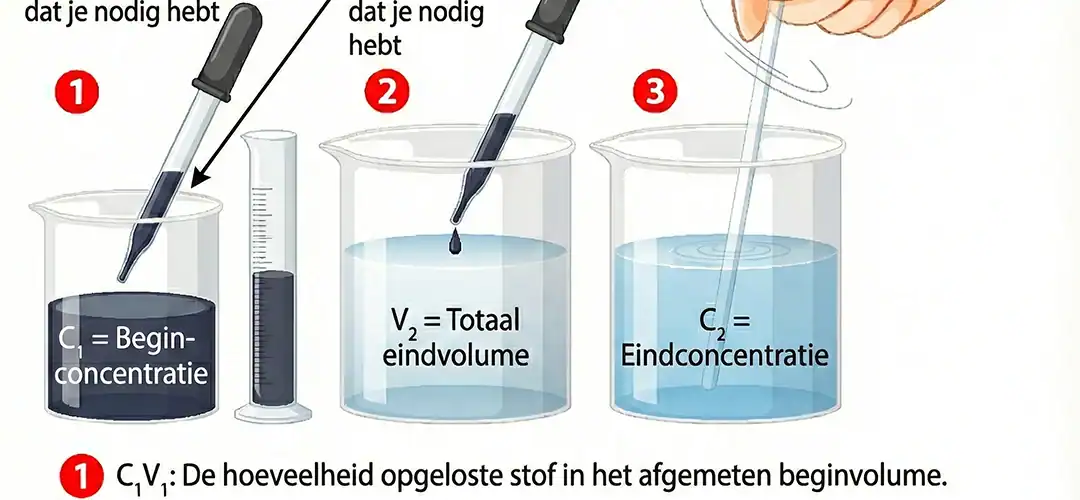
- C₁ = Anfangskonzentration (Stammlösung)
- V₁ = benötigtes Volumen der Stammlösung
- C₂ = gewünschte Konzentration nach Verdünnung
- V₂ = Gesamtvolumen der verdünnten Lösung
Warum funktioniert diese Formel? Weil die Menge des gelösten Stoffes vor und nach der Verdünnung gleich bleibt. Man ändert lediglich das Volumen, in dem sich der gelöste Stoff verteilt.
Beispielrechnung: Herstellung einer verdünnten Lösung
Machen wir das konkret.
Ziel: Herstellung von 100 ml einer 0,1 M Lösung aus einer 1,0 M Stammlösung.
Schritt 1: Schreiben Sie auf, was Sie wissen.
- C₁ = 1,0 M
- C₂ = 0,1 M
- V₂ = 100 ml
- V₁ = unbekannt (wir werden dies berechnen)
Schritt 2: Verwenden Sie die Formel
C₁V₁ = C₂V₂
Schritt 3: Löse zu V₁ auf
V₁ = (C₂ × V₂) / C₁
V₁ = (0,1 × 100) / 1,0
V₁ = 10 ml
Schritt 4: Die Berechnung in praktische Aktionen im Labor umsetzen
- Messen Sie 10 ml der 1,0 M Stammlösung ab.
- Überführen Sie dies in einen Messkolben.
- Mit destilliertem Wasser auffüllen, bis das Gesamtvolumen 100 ml beträgt.
- Gründlich vermischen.
Hinweis: Es werden nicht exakt 90 ml Wasser hinzugegeben. Das Gesamtvolumen beträgt maximal 100 ml. Dieses kleine Detail führt häufig zu Fehlern.
Mit anderen Lösungsmitteln verdünnen (nicht nur mit Wasser).
Wasser ist das am häufigsten verwendete Lösungsmittel in Schullaboren, doch viele chemische Lösungen werden mit anderen Flüssigkeiten wie Isopropanol , Aceton , Ethanol oder speziellen organischen Lösungsmitteln verdünnt. Das Grundprinzip bleibt dabei gleich: Die Konzentration wird durch Erhöhung des Gesamtvolumens bei gleichbleibender Stoffmenge reduziert. Die Arbeit mit nicht-wässrigen Lösungsmitteln erfordert jedoch einige zusätzliche Überlegungen.
Wie führt man eine Verdünnung praktisch durch?
Wenn die Berechnung stimmt, ist die Umsetzung unkompliziert. Ein typisches Vorgehen:
- Zuerst die Stammlösung mit einer Pipette oder einem Messzylinder abmessen.
- Überführen Sie diese in einen Messkolben oder ein geeignetes Gefäß.
- Lösungsmittel langsam zugeben.
- Stoppen Sie, sobald Sie die Endlautstärkemarkierung erreicht haben.
- Schließen und durch Schwenken oder Drehen vorsichtig vermengen.
Genauigkeit ist hier wichtiger als Geschwindigkeit. Eile führt meist zu Mengenfehlern oder Verschüttungen.

Häufige Fehler
Jeder macht sie am Anfang. Das sind die Klassiker:
Verwechslung von hinzugefügtem Volumen mit Endvolumen
Wenn das Endvolumen 100 ml beträgt, ist darin auch der Inhalt des Kolbens enthalten.
Einheitenumrechnung vergessen
Konzentrationen werden häufig in mol/L und Volumina in mL angegeben. Achten Sie auf eine einheitliche Berechnung.
zu früh runden
Berücksichtigen Sie bei der Berechnung zusätzliche Dezimalstellen und runden Sie erst am Ende.
Glücksspiel statt Berechnung
Verdünnen scheint einfach, aber das Schätzen von Verhältnissen führt oft zu falschen Konzentrationen.
Die meisten Fehler entstehen dadurch, dass Schritte ausgelassen werden, nicht weil die Chemie zu schwierig ist.
Was ist eine Verdünnungsreihe?
Eine Verdünnungsreihe ist eine schrittweise Methode zur Herstellung sehr niedriger Konzentrationen. Anstatt direkt von einer starken zu einer extrem schwachen Lösung überzugehen, arbeitet man stufenweise.
Zum Beispiel:
- Erste Verdünnung: 1 Teil Lösung + 9 Teile Wasser → 1:10
- Zweite Verdünnung: Den gleichen Schritt wiederholen → 1:100
- Dritte Verdünnung: Vorgang wiederholen → 1:1000
Diese Methode wird häufig in biologischen Experimenten und in der analytischen Chemie eingesetzt, da sie bei sehr niedrigen Konzentrationen genauer ist.
Es ist, als würde man eine Lampe langsam dimmen, anstatt sie sofort auf die niedrigste Stufe herunterzudrehen.
Sicherheitshinweise beim Verdünnen von Chemikalien
Auch für einfache Verdünnungen gelten die Grundregeln:
- Im Labor ist stets Schutzbrille und Schutzhandschuhe zu tragen.
- Konzentrierte Säure wird in Wasser gegeben, niemals umgekehrt.
- Verdünnte Lösungen sofort mit Konzentration und Datum beschriften.
- Verwenden Sie sauberes Glasgeschirr, um Verunreinigungen zu vermeiden.
Sicherheitsregeln haben ihren Sinn. Mit der Zeit werden sie zur Routine.
Kurz zusammengefasst: Verdünnungs-Spickzettel
Denken Sie beim Üben daran:
- Durch Verdünnung wird die Konzentration durch Zugabe von Lösungsmittel verringert.
- Die Menge des gelösten Stoffes bleibt gleich.
- Verwenden Sie die Formel C₁V₁ = C₂V₂.
- Auf das Endvolumen verdünnen, nicht basierend auf einer geschätzten Zugabe.
- Arbeiten Sie präzise und beschriften Sie alles.
Verdünnen mag zunächst schwierig erscheinen, aber im Grunde geht es um kontrolliertes Mischen. Verstehen Sie, warum die Formel funktioniert, befolgen Sie die Schritte konsequent, und Sie werden feststellen, dass die meisten Probleme demselben Muster folgen. Üben Sie ein paar Beispiele, und es wird zur Routine statt zum Stressfaktor.